Náplň podkapitoly:
1. Úvod do metabolismu kostní tkáně
2. Remodelace kostí
3. Regulace metabolismu kostí
4. Biochemické markery kostního metabolismu
5. Vybraná onemocnění kostí
_
Úvod do metabolismu kostní tkáně
Kosti plní v lidském těle mnoho funkcí:
1) Mechanická – opora pro svaly, chrání kostní dřeň
2) Zásobárna kalcia a fosfátů – zcela zásadním způsobem ovlivňují jejich metabolismus
3) Pufr 3. linie – u dlouhodobé metabolické acidózy uvolňují fosfát a bikarbonát
Složení kosti
1) Buňky
a) Syntezující novou kostní tkáň: osteoblasty, osteocyty
b) Odbourávající kostní tkáň: osteoklasty
2) Mezibuněčná matrix
a) Organická složka: kolagen typu I a nekolagenní proteiny (např. osteokalcin, protein S)
b) Anorganická složka: apatit – krystalická forma Ca3(PO4)2 (hydroxyapatit – Ca10(PO4)6(OH)2, apatit karbonát – Ca10(PO4)6CO3 či fluoroapatit – Ca10(PO4)6F2)
Osteoblasty
Osteoblasty pocházejí z mezenchymových buněk kostní dřeně. Jedná se o vysoce proteosynteticky aktivní buňky, které vykazují zvýšenou aktivitu alkalické fosfatázy. Jejich základní funkcí je tvorba kostní matrix a její mineralizace. Činnost osteoblastů ovlivňuje mnoho hormonů (např. parathormon, kalcitriol či estrogeny), či mechanické faktory (jejich membrány obsahují mechanoreceptory).
Osteoklasty
Osteoklasty pocházejí z buněk monocytomakrofágové řady. Obsahují četné lyzosomy s proteolytickými enzymy (kolagenázu, katepsiny atd.) a izoenzym kyselé fosfatázy. Membrána osteoklastů obsahuje protonovou pumpu (schopna snížit pH ze 7 na 4) a vybrané receptory (např. pro kalcitonin). Aktivitu osteoklastů řídí i signály z osteoblastů. Jejich základní funkcí je resorpce kosti (vede souběžně ke zvyšování kalcemie).
_
Remodelace kostí
Během celého života probíhá neustálá přestavba kostí. Je velmi významná, protože podmiňuje přizpůsobení kosti na proměny jejího zatížení, zachovává její celistvost (reparuje drobná poškození) a spolupodílí se na metabolismu Ca2+ a fosfátů.
Ve 25 letech dosáhneme tzv. vrcholu kostní hmoty – PBM (peak bone mass). Poté následuje individuálně dlouhá (průměrně 5 let) vyrovnaná remodelace, což znamená, že intenzita resorpce se rovná intenzitě novotvorby kosti. Po této době nastupuje trvalý úbytek kostní hmoty, který činí přibližně 0,5 % za rok – převažuje odbourávání kostí nad jejich novotvorbou. U žen dochází po menopauze ke zvýšení rychlosti úbytku kostní tkáně – riziko rozvoje osteoporózy. Obézní lidé naopak netrpí tak výrazným úbytkem, protože jejich kosti jsou trvale více zatěžovány – zátěž je jedním z hlavním regulujících mechanismů. Přestavbu kosti obecně modulují endokrinní a parakrinní signály, mechanické podněty a hladiny vápníků a fosfátů.
Cyklus remodelace kostí zahrnuje přibližně čtyři měsíce a můžeme ho rozdělit do třech fází:
1) Stimul, např. fyzická zátěž
2) Resorpce kosti činností osteoklastů
3) Tvorba kostní tkáně činností osteoblastů
_
Regulace metabolismu kostí
Metabolismus kostní tkáně je regulován mnoha endokrinními a parakrinními signály. Endokrinní signály si ještě z didaktického hlediska rozdělíme na hormony ovlivňující metabolismus vápníku a fosfátů a na ostatní systémové hormony.
Hormony metabolismu vápníku a fosfátů
Problematika kalciofosfátového metabolismu je detailně probrána v Kapitole 7. Na tomto místě se omezíme pouze informace o vlivu těchto hormonů na metabolismus kostí.
V lidském těle hrají klíčovou roli v regulaci obsahu Ca2+ a fosfátů tři hormony – parathormon, kalcitriol a kalcitonin.
1) Parathormon
Parathormon stimuluje odbourávání (resorpci) kosti zvýšením aktivity osteoklastů (stimuluje transformaci monocytů na osteoklasty). Výsledkem je zvýšené uvolňování Ca2+ a fosfátů z kosti.
2) Kalcitonin
Kalcitonin inhibuje aktivitu osteoklastů (tlumí transformaci monocytů na osteoklasty), čímž snižuje resorpci kosti a výsledkem je zvýšené ukládání Ca2+ v kostech.
3) Kalcitriol (1,25-dihydroxycholekalciferol, derivát vitaminu D)
Kalcitriol stimuluje v tenkém střevě syntézu bílkovin umožňujících absorpci Ca2+ a fosfátů. Tím zajišťuje dostupnost Ca2+ a fosfátů pro stavbu kosti. Souběžně aktivuje osteoblasty k syntéze kolagenu.
Další endokrinní signály
1) Estrogeny
Estrogeny účinkují obdobně jako kalcitonin. Inhibují tedy kostní resorpci – inhibují aktivitu osteoklastů přes lokální faktory.
2) Růstový hormon
Růstový hormon stimuluje kostní tvorbu skrze tvorbu lokálních růstových faktorů – insulin-like growth factors (somatomediny – IGF-1 a IGF-2).
Podrobnější informace o insulin-like growth factors viz Kapitola 11.
3) Inzulin
Inzulin zvyšuje syntetickou aktivitu osteoblastů. Při neléčeném diabetu mohou nastat ztráty kostní hmoty.
4) Glukokortikoidy
Glukokortikoidy snižují novotvorbu kosti (inhibují proteosyntézu v osteoblastech a jejich diferenciaci).
5) Hormony štítné žlázy
Hormony štítné žlázy stimulují osteoklasty, aktivují kostní remodelaci. Při jejich nadprodukci se může vyvinout až osteoporóza.
Přehled endokrinní regulace metabolismu kostí
|
Hormon |
Resorpce |
Tvorba |
| PTH |
↑ |
↑ |
| Kalcitriol |
↑ |
↑ |
| Kalcitonin |
↓ |
– |
| Pohlavní hormony |
↓ |
↓ |
| Růstový hormon |
– |
↑ |
| Inzulin |
– |
↑ |
| Glukokortikoidy |
↑ |
↓ |
| Hormony ŠŽ |
↑ |
↑ |
_
Parakrinní signály modulující metabolismus kostí
1) Faktory stimulující osteoblasty
a) Bone morphogenic factor (BMF)
b) Insulin-like growth factor 1 (IGF-1)
c) Platelet-derived growth factor (PDGF)
d) Fibroblast growth factor (FGF)
2) Faktory stimulující osteoklasty
a) M-Colony stimulating factor (M-CSF)
b) Interferony (INF-γ) a některé interleukiny (IL-1, IL-6 atd.)
Přehled parakrinní regulace metabolismu kostí
|
Lokální působky |
Resorpce |
Tvorba |
| Růstové faktory |
↑ |
↑ |
| Faktory z osteoblastů |
↓ |
↑ |
| Zánětlivé cytokiny |
↑ |
↓ |
_
Biochemické markery kostního metabolismu
Laboratorními markery kostního metabolismu může být mnoho látek. Jednak mezi ně patří ionty – Ca2+ (celkové 2,25-2,75 mmol/l, ionizované 1,1-1,4 mmol/l) a fosfáty (0,7-1,5 mmol/l), jednak hormony ovlivňující kostní metabolismus (např. parathormon, kalcitonin, vitamin D / kalcitriol, estrogeny, glukokortikoidy atd.). Kromě nich ale existují i specifické markery kostního metabolismu.
Rychlost tvorby a resorpce kosti se dá nejlépe posoudit podle produktů vznikajících v metabolismu organických složek kostní matrix (například při syntéze a degradaci kolagenu) a některých enzymů. Podle toho, kdy jsou tyto markery zvýšené, je rozdělujeme na markery novotvorby kosti a markery odbourávání kosti.
Markery novotvorby kosti
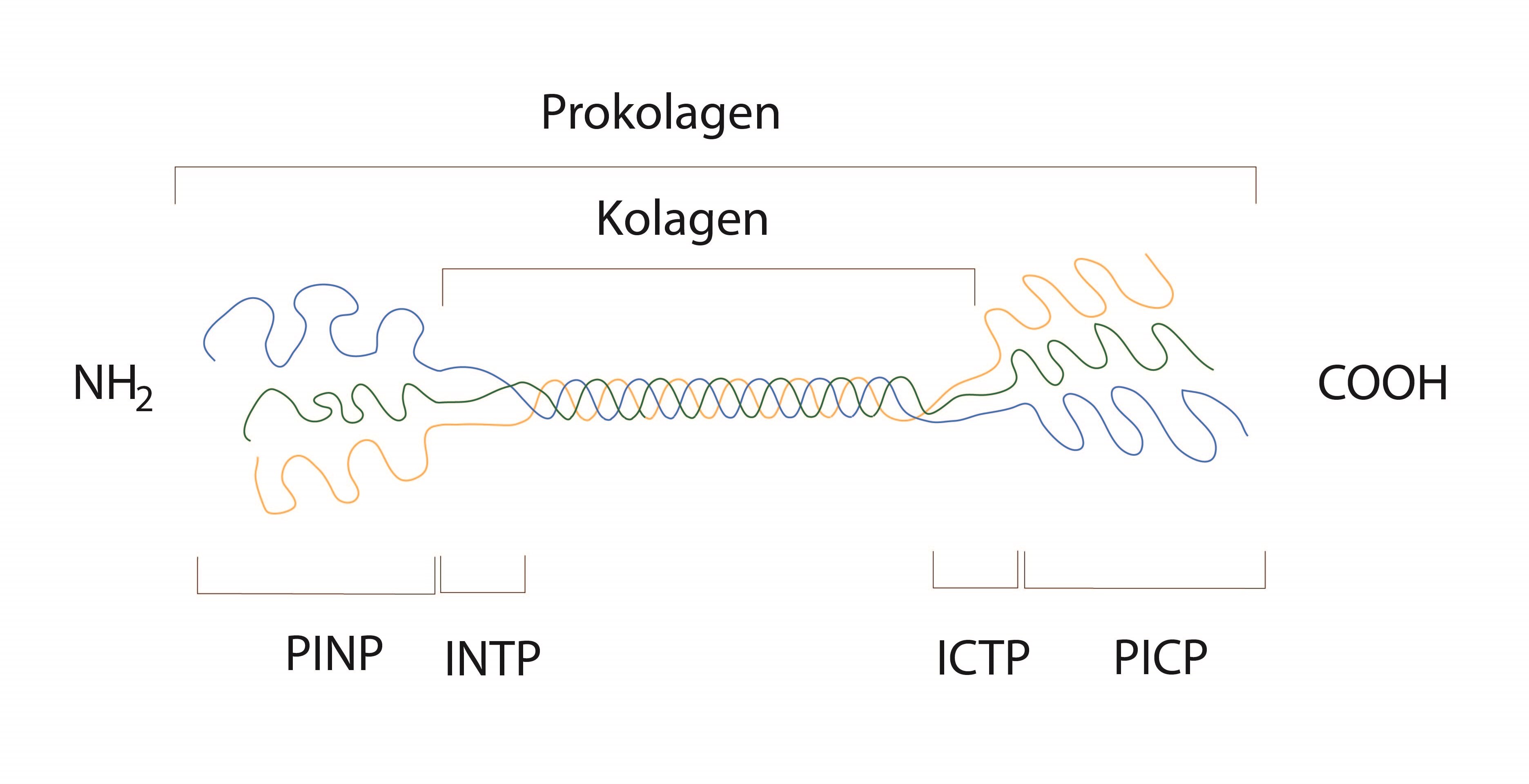
Mezi markery novotvorby kosti patří například kostní izoenzym alkalické fosfatázy (ALP), terminální propeptidy prokolagenu typu I (U-PINP, U-PICP) či sérový osteokalcin.
Terminální propeptidy prokolagenu typu I vznikají odštěpením propeptidu z molekuly prokolagenu.
Osteokalcin (Gla protein) je nekolagenní protein kostní matrix, jehož molekula obsahuje zbytky kyseliny glutamové karboxylované na γ-uhlíku. Osteokalcin váže hydroxyapatit.
Markery odbourávání kosti
Mezi markery odbourávání kosti patří například kostní izoenzym kyselé fosfatázy (tartát rezistentní), karboxyterminální telopeptidy kolagenu (U-ICTP), močový hydroxyprolin či močový deoxypyridinolin (vznikají degradací příčných vazeb zralých kolagenních fibril, peptidové fragmenty kolagenu s deoxypyridinolinovými spojkami, patří mezi pyridiniové sloučeniny).
Karboxyterminální telopeptidy kolagenu vznikají degradací kolagenních vláken.
_
Vybraná onemocnění kostí
Osteoporóza
Osteoporóza (nesprávně nazývána řídnutí kostí) je systémové onemocnění. Dochází při ní k úbytku anorganické i organické kostní hmoty, který vyúsťuje ve sníženou kostní denzitu a zvýšenou fragilitu kostí. Následkem je tedy zvýšené riziko fraktur. Rozlišujeme tzv. primární osteoporózu, u níž neznáme příčinu (u žen po menopauze či osteoporóza ve starším věku) a sekundární osteoporózu, kde příčinu známe (např. endokrinní, léky, imobilizace). Osteoporóza je závažný zdravotnický problém – postihuje 7-8 % populace ČR a přibližně 1/3 žen po menopauze.
Osteomalacie (v dospělosti) / rachitida (v dětství)
Toto onemocnění je vyvoláno poruchou mineralizace osteoidu. Dochází převážně k úbytku anorganické kostní hmoty (dekalcifikace kostí), jejímž následkem je měknutí kostí a jejich deformity (pro křivici jsou typické deformity lebky, páteře, hrudníku a dlouhých kostí).
Nejčastější příčinou je nedostatek vitaminu D (jeho aktivní formou je kalcitriol), jehož význam pro metabolismus kostí byl uveden výše. Jeho deficit vyústí v hypokalcemii, na níž tělo reaguje zvýšeným vyplavením parathormonu, který kromě jiného vychýlí poměr Ca2+ / fosfáty (nárůst kalcemie a posked fosfatemie). Vzniklý nepoměr znesnadňuje mineralizaci osteoidu. Příčinou nedostatku vitaminu D může být například jeho nedostatečný příjem či onemocnění ledvin.
Autoři podkapitoly: Josef Fontana a Petra Lavríková