Náplň podkapitoly:
1. Tvorba a funkce likvoru
2. Složení likvoru
3. Hematoencefalická bariéra a hematolikvorová bariéra
_
Tvorba a funkce likvoru
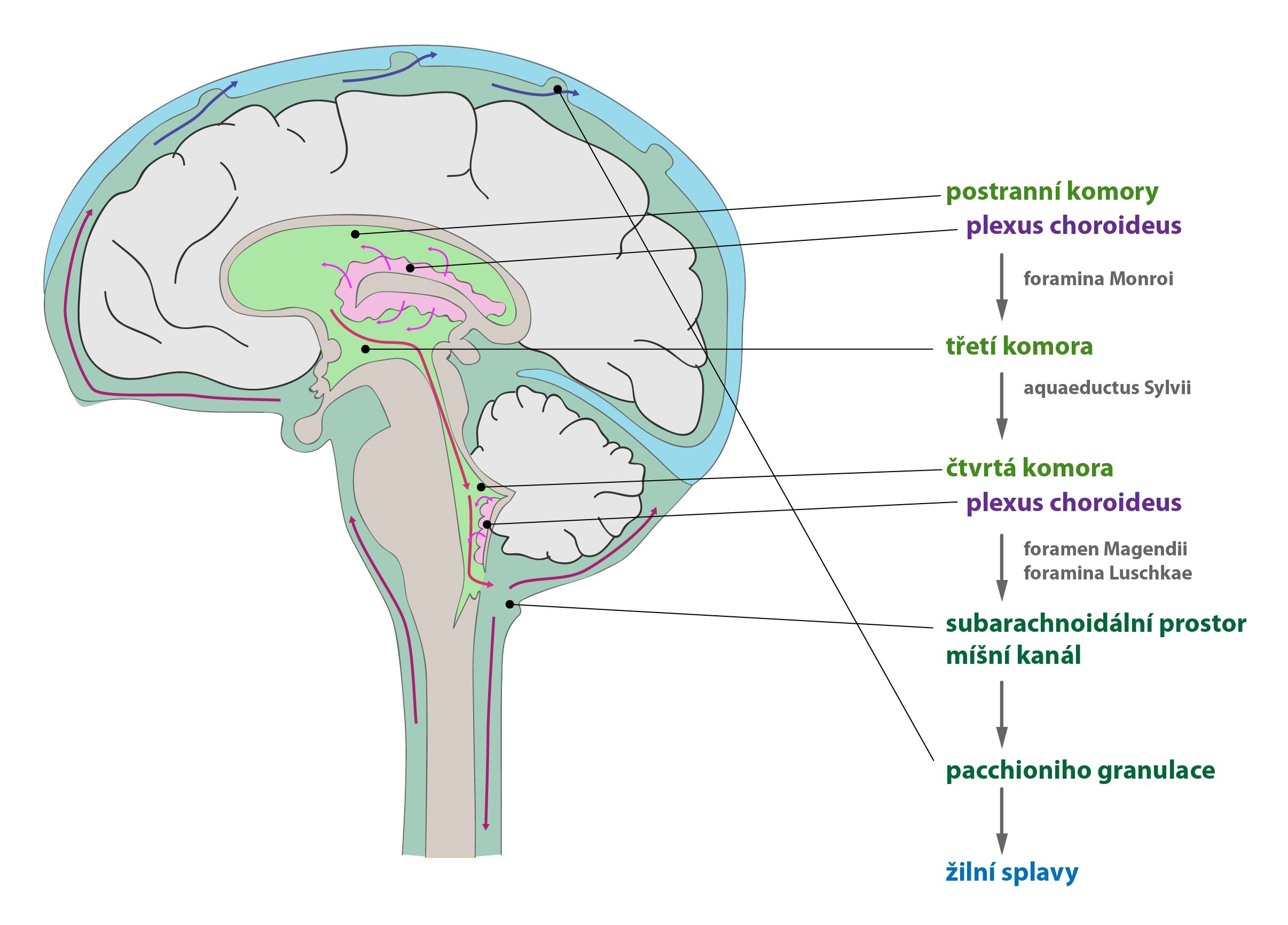
Likvor (mozkomíšní mok, liquor cerebrospinalis, CSF – cerebrospinal fluid), čirá, bezbarvá tekutina, se v CNS nachází jednak intracerebrálně, v komorovém systému mozku (asi 20 % celkového objemu) a jednak extracerebrálně v subarachnoidálním prostoru (zbylých 80 % objemu).
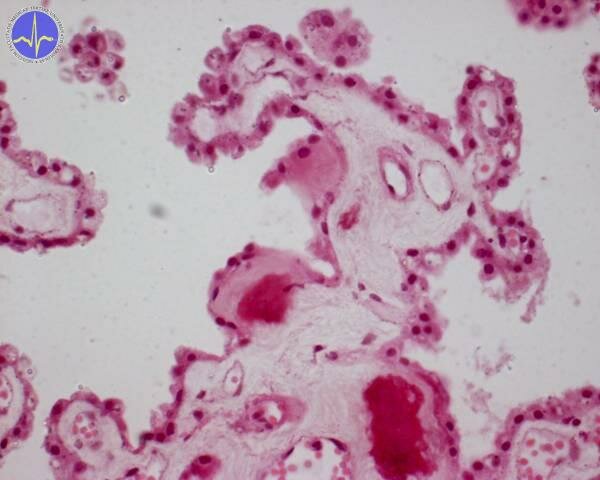
Celkový objem mozkomíšního moku činí asi 150 ml, za den se ho vyprodukuje přibližně 450 ml (obmění se třikrát denně). Likvor je tvořen sekrecí, buňkami choroidálních plexů a ependymu komor (asi 50-70 % celkového vytvořeného objemu) a zbytek se tvoří ultrafiltrací plazmy přes choroidální kapiláry.
Choroidální plexus
Jeho cirkulace směřuje z postranních komor přes foramina Monroi do třetí komory. Přes aquaeductus Sylvii přetéká do čtvrté komory a z ní odtéká do subarachnoidálního prostoru nepárovým foramen Magendii a párovými foramina Luschkae. Likvor nacházející se v subarachnoidálním prostoru tedy obklopuje mozek a míchu. Část likvoru ze čtvrté komory se také dostává dál do centrálního kanálu míchy.
Resorpce likvoru probíhá v arachnoidálních klcích granulationes arachnoideae (Pacchioniho granulace). Jedná se o výběžky arachonidei přes dura mater, které zasahují až do nitrolebečních žilních splavů mozku a umožňují tak odtok likvoru do krevní cirkulace.
Důležité je zachování správné rovnováhy mezi sekrecí, cirkulací a resorpcí moku. V případě vzniklé nerovnováhy dochází k hromadění moku v některé části systému a vzniká hydrocefalus. Pokud se likvor hromadí v komorovém systému, hovoříme o vnitřním hydrocefalu. Jestliže se hromadí v oblasti subarachnoidálního prostoru, jde o hydrocefalus vnější.
Likvor plní následující funkce:
1) Mechanická a podpůrná
Tím, že je mozek v podstatě ponořen v mozkomíšním moku, se jeho reálná hmotnost (kolem 1500 g) sníží na ekvivalent přibližně 25 g. Tak je mozek chráněn před poškozením svou vlastní vahou.
2) Ochranná
Likvor působí jako tlumič nárazů a otřesů, chrání mozek před prudkými změnami tlaku či teploty a obsahem komponent imunitního systému (leukocyty, Ig, …) poskytuje také ochranu před různými patogeny.
3) Metabolická
Likvor pomáhá udržovat správné složení prostředí obklopující buňky nervové tkáně (homeostáza), částečně zabezpečuje přísun živin a odvod zplodin metabolismu a také je médiem, přes které mohou difundovat různé signální molekuly (například neurotransmitery).
Je třeba si uvědomit, že objem tkání a tekutin uložených v lebce je limitován objemem kostní schránky. Platí tzv. Monroe-Kellyova doktrína, která říká, že objem intrakraniálního prostoru je konstantní, a proto jeho jednotlivé složky (krev, mozkomíšní mok a nervová tkáň) existují ve stavu objemové rovnováhy. Jakýkoli nárůst jedné komponenty (například při intrakraniálním krvácení, hydrocefalu nebo růstu tumoru) je kompenzován poklesem objemu ostatních komponent. Mozkomíšní mok má v rámci tohoto systému funkci jakéhosi pufru (i když s ne příliš velkou kapacitou), který jako první kompenzuje nárůst objemu zbylých dvou kompartmentech. V menší míře má tuto schopnost i krevní cirkulace mozku, ale při jejím přílišném omezení vyvstává riziko hypoxického poškození mozkové tkáně.
_
Složení likvoru
Fyziologické hodnoty
Složení mozkomíšního moku se kvalitativně příliš neliší od plazmy, odlišuje se však kvantitativně. Přípona -rachie označuje koncentraci dané látky v mozkomíšním moku – např. glykorachie (koncentrace glukózy v mozkomíšním moku) či proteinorachie (koncentrace celkové bílkoviny v mozkomíšním moku).
Základním vyšetřením, kterým zjišťujeme koncentrace jednotlivých látek v moku, je jeho punkce. Ta se obvykle provádí v lumbální oblasti (mezi L4 a L5), vzácný je subokcipitální přístup. Odebírají se 4 vzorky (po přibližně 2 ml):
1) Biochemie: ionty, glukóza, laktát, proteiny včetně ELFO
2) Cytologie
3) Mikrobiologie: kultivace, případně PCR
4) 1 záložní vzorek (uchovává se při 4 °C)
Při odběru se také může měřit tlak mozkomíšního moku, jehož hodnota dosahuje při lumbální punkci u pacienta ležícího na boku přibližně 8-15 mmHg (10-18 cm H2O) a u sedícího pacienta 16-24 mmHg (20-30 cm H2O).
Fyziologické nálezy shrnují následující tabulky:
1) Ionty
|
Látka |
Hodnota |
% z plazmatické hodnoty |
| pH |
7,28-7,32 |
|
| Osmolarita |
285 mosm/l |
|
| Specifická hmotnost |
1003-1008 |
|
| Na+ |
135-150 mmol/l |
|
| K+ |
2,0-3,0 mmol/l |
|
| Ca2+ |
1,1-1,25 mmol/l |
~50 % |
| Cl– |
115-130 mmol/l |
>100 % |
2) Živiny a proteiny
|
Látka |
Hodnota |
% z plazmatické hodnoty |
| Glukóza (glykorachie) |
2,2-4,2 mmol/l |
~60 % |
| Proteiny (proteinorachie) |
0,1-0,40 g/l |
~1 % (zejména malé proteiny, imunoglobuliny – IgG, IgM) |
| Laktát |
1,1-2,0 mmol/l |
|
| Urea |
3-6,5 mmol/l |
|
| Lipidy |
10-30 mg/l |
3) Buňky
|
Druh buněk |
Hodnota |
| Erytrocyty |
0 / mm3 |
| Lymfocyty |
0-5 / mm3 |
| Bakterie |
0 / mm3 |
Patologické stavy
Mnohá onemocnění CNS způsobují změny ve složení a koncentracích jednotlivých složek mozkomíšního moku. Jeho vyšetření je proto významné v diferenciální diagnostice a pro potvrzení diagnózy těchto onemocnění.
Mezi nejčastější příčiny změn složení mozkomíšního moku patří různé formy meningitid:
1) Hnisavá (purulentní) bakteriální meningitida
Pro hnisavou (purulentní) bakteriální meningitidu je charakteristický hnisavý vzhled moku, přítomnost tisíců neutrofilů na mm3 likvoru, pokles koncentrace glukózy (kterou bakterie využívají jako zdroj energie), a naopak nárůst laktátu (jejž produkují bakterie ve svém metabolismu). Objevuje se též výrazný nárůst proteinů (bakteriální fragmenty, Ig, …).
2) Virová aseptická meningitida
Virová aseptická meningitida se běžně vyznačuje menším rozsahem vyvolávaných změn. Koncentrace glukózy a laktátu je v normě, bílkoviny jsou zvýšené jen mírně. V moku nacházíme převážně lymfocyty, řádově ve stovkách buněk na mm3.
Pro některá degenerativní onemocnění (například roztroušená skleróza – RS čili sclerosis multiplex) bývá charakteristická přítomnost tzv. oligoklonálních pruhů. Jedná se o výrazné pruhy proteinů (nebo jejich fragmentů) viditelné na elektroforéze, které představují různé druhy protilátek tvořené plazmatickými buňkami.
Hematologické malignity mohou způsobit infiltraci moku nádorovými (například leukemickými) buňkami, které se zjistí při cytologickém vyšetření.
_
Hematoencefalická bariéra a hematolikvorová bariéra
Hematoencefalická bariéra
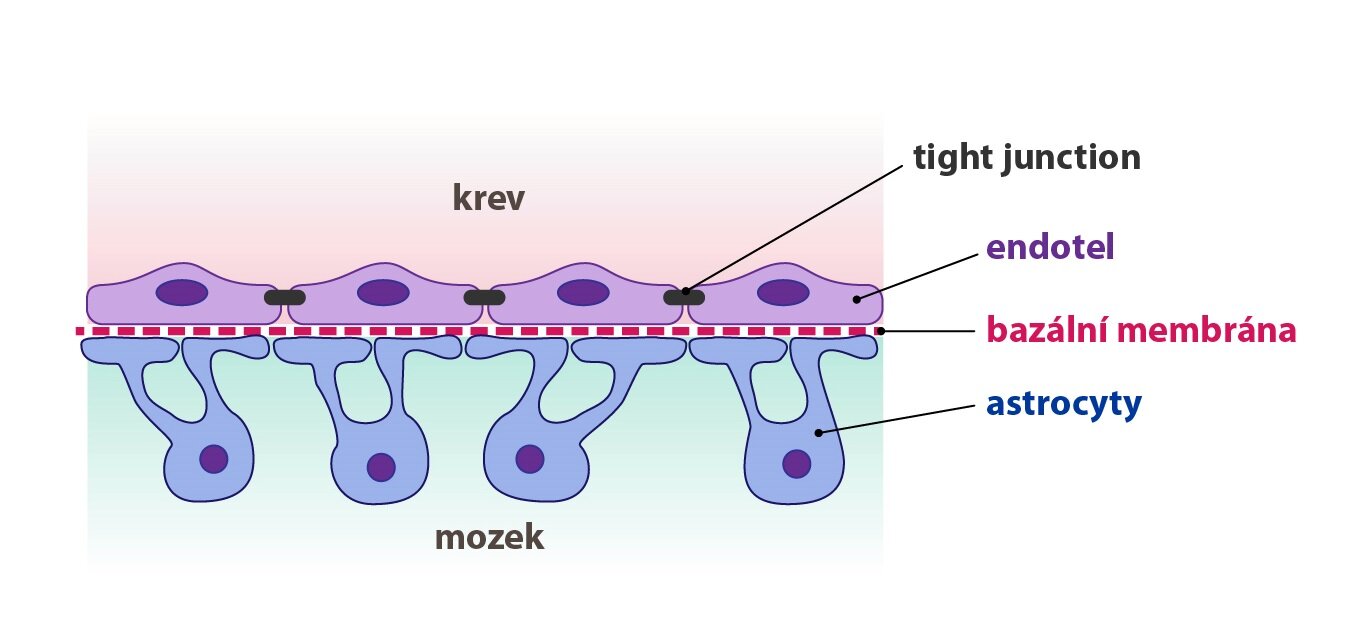
Termín hematoencefalická bariéra (HEB) označuje bariéru oddělující mozkovou tkáň a krevní oběh. Její strukturní podklad tvoří tři části:
1) Vrstva endotelových buněk vzájemně spojených prostřednictvím tight junctions a neobsahujících fenestrace (v jiných tkáních běžně přítomné)
2) Bazální membrána, jež je tvořena bazální laminou endotelových buněk a astrocytů
3) Výběžky astrocytů – tzv. pedikly, které nasedají na bazální membránu
Základní funkcí HEB je ochrana tkáně CNS (především neuronů) vůči různým noxám, které by za normálních okolností mohly do tkáně CNS pronikat. Selektivita HEB tedy brání průniku mnoha škodlivých látek, ale na druhé straně umožňuje průnik látek pro mozek potřebných. Obecně přes HEB nepronikají látky hydrofilní, pokud nemají na endotelových buňkách a astrocytech příslušné transportéry. Hydrofóbní povaha bariéry naopak obecně umožňuje průnik látek lipofilních.
1) Volně, prostřednictvím pasivní difúze, přes HEB procházejí:
a) malé molekuly: H2O, O2, CO2, NH3, etanol
b) lipofilní látky: steroidní hormony
2) Selektivní transportéry pro facilitovanou difúzi či aktivní transport mají například:
a) glukóza: GLUT-1
b) aminokyseliny
3) Některé makromolekuly procházejí prostřednictvím pinocytózy
Přítomnost HEB má některé významné klinické dopady. Kromě toho, že HEB brání průniku mikroorganismů a vzniku infekce v oblasti CNS, omezuje i přestup protilátek a antibiotik, což může terapii případné infekce výrazně znesnadnit. Mimo zmíněná antibiotika existuje celá řada jiných léků a látek, které přes HEB neprostupují. Příkladem je neurotransmiter dopamin, který se tedy nemůže přímo používat v léčbě Parkinsonovy nemoci (způsobené nedostatkem dopaminu v bazálních gangliích mozku). Místo něj se využívá jeho prekurzor – L-DOPA, která HEB přestupuje a na dopamin je přeměněna až v mozkové tkáni.
Encefalopatie při nekonjugované hyperbilirubinemii (tzv. kernikterus) vzniká u novorozenců v důsledku ještě nedostatečně vyvinuté HEB, jež umožňuje přestup bilirubinu do mozkové tkáně. U dospělých s plně vyvinutou a funkční HEB se s toto poruchou obvykle nesetkáváme.
V mozku ale existují i oblasti bez ochrany HEB. Jedná se o chemorecepční zóny, jejichž úlohou je kontrolovat složení krve. Patří sem například:
1) Subfornikální orgán: obsahuje osmoreceptory regulující sekreci ADH
2) Organum vasculosum laminae terminalis (OVLT): obsahuje osmoreceptory regulující sekreci ADH a vyvolávající pocit žízně
3) Area postrema: obsahuje chemoreceptory, které jsou součástí centra pro zvracení
Hematolikvorová bariéra
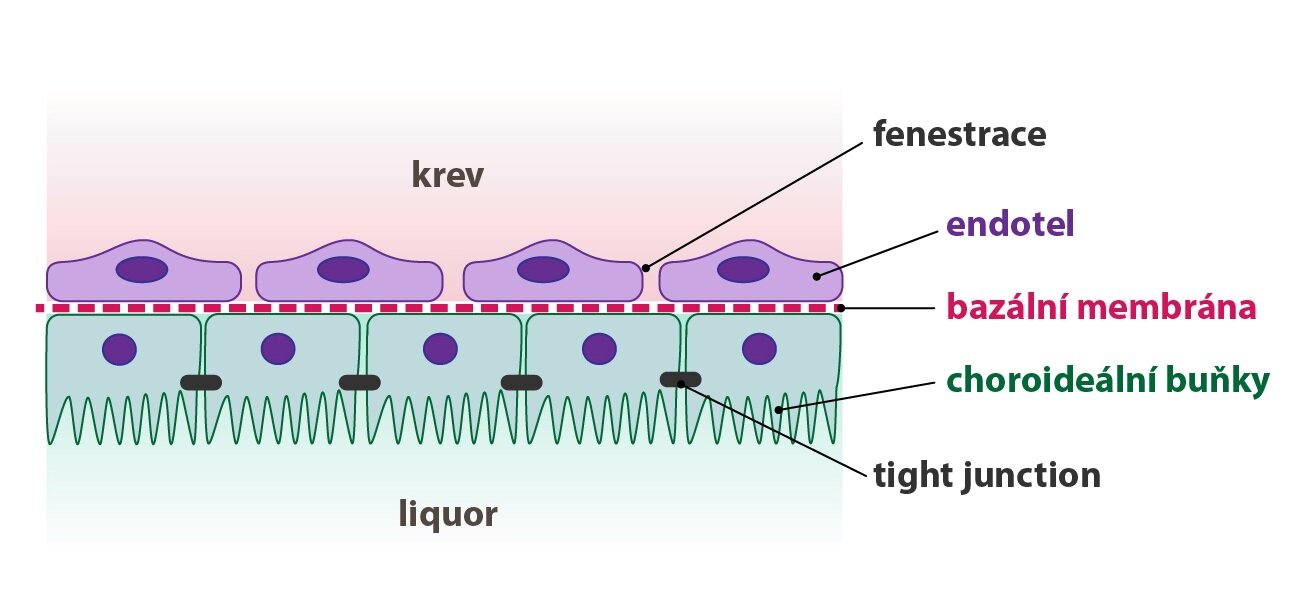
Hematolikvorová bariéra odděluje mozkomíšní mok a krev. Podobně jako hematoencefalickou bariéru ji strukturně tvoří tři složky:
1) Choroidální epiteliální buňky spojené prostřednictvím tight junctions (ale prostupnější než obdobné spoje mezi endoteliálními buňkami mozkových kapilár) a secernující mozkomíšní mok. Na straně obrácené směrem k likvoru je jejich povrch zvětšen přítomností výběžků – tzv. mikrovili
2) Bazální membrána
3) Vrstva endotelu kapilár pia mater obsahující fenestrace
Hematolikvorová bariéra plní úkol omezovat vstup látek z krve přímo do likvoru. Bariéra je ale permeabilnější než HEB, a mnohé proteiny krevní plazmy se tedy dostávají prostřednictvím pinocytózy nebo aktivním transportem do moku. Jejich koncentrace je zde ale nižší než v plazmě. Porucha hematolikvorové bariéry se proto projeví vzestupem proteinů krevní plazmy v moku. Transport se děje i opačným směrem, a tak se látky z likvoru mohou dostat zpátky do cirkulace.
Autoři podkapitoly: Petra Lavríková a Josef Fontana