Náplň podkapitoly:
1. Nejvýznamnější chemické reakce v metabolismu
2. Základy regulace metabolických drah
Nejvýznamnější chemické reakce v metabolismu
Metabolické dráhy lidského organismu tvoří rozsáhlou síť více či méně propojených reakcí, které často sdílejí společné meziprodukty. Chemické přeměny jednotlivých látek, k nimž v rámci reakcí dochází, obvykle třídíme podle určitého obecného mechanismu společného pro všechny látky podstupující danou reakci. Například u dekarboxylace se jedná o odštěpení CO2 z karboxylové skupiny, přičemž substrátem mohou být různé karboxylové kyseliny. V této kapitole uvedeme nejvýznamnější druhy chemických reakcí v metabolismu a jejich typické příklady.
Alkoholy, karbonylové sloučeniny a karboxylové kyseliny
Alkoholy, karbonylové sloučeniny a karboxylové kyseliny patří mezi významné substráty mnoha reakcí metabolických drah organismů.
Alkoholy obsahují funkční skupinu -OH. Podle jejího počtu v molekule mohou být alkoholy jedno-, dvou- nebo vícesytné. Dále je lze dělit podle toho, na jaký atom uhlíku se -OH skupina váže, a z tohoto hlediska pak rozlišujeme primární (R-CH2-OH), sekundární (R1-CH(OH)-R2) a terciární (C-R1R2R3(OH)) alkoholy.
Aldehydy společně s ketony tvoří skupinu karbonylových sloučenin. Funkční skupinou aldehydů je skupina –CHO, u ketonů C=O.
Z této skupiny jsou pro organismus pravděpodobně nejvýznamnějšími substráty reakcí karboxylové kyseliny charakterizované přítomností funkční skupiny -COOH, či jejich deriváty.
Mezi významné reakce alkoholů, aldehydů a karboxylových kyselin patří:
1) Tvorba aniontů a acylů odvozených od karboxylových kyselin
2) Dehydrogenace a hydrogenace (oxidace a redukce)
3) Esterifikace
1) Tvorba aniontů a acylů odvozených od karboxylových kyselin
Karboxylová skupina je schopna disociace, přičemž míru disociace pro jednotlivé kyseliny udává disociační konstanta. Karboxylové kyseliny patří většinou mezi kyseliny slabé, což znamená, že jejich disociace je jen parciální. Z kyseliny tak vzniká aniont (skupina -COO–).
Po odštěpení celé -OH skupiny z karboxylové skupiny vzniká její acyl.
2) Dehydrogenace a hydrogenace (oxidace a redukce)
Během chemické reakce zvané dehydrogenace dochází k odstranění -H z molekuly. Vodík, který tímto procesem získáme, můžeme následně využít při tvorbě protonového gradientu v mitochondriích a k zisku energie (ATP). Vnesení vodíku do molekuly se nazývá hydrogenace. V organismu se dehydrogenace a hydrogenace vyskytují například při:
a) Oxidacích jednoduchých vazeb na vazby dvojné
b) Vzájemných přeměnách alkoholů – aldehydů / ketonů – karboxylových kyselin
a) Oxidace jednoduchých vazeb na vazby dvojné
Obecné schéma reakce lze vyjádřit takto:
-CH2-CH2– ↔ -CH=CH- + 2H+ + 2e–
Tyto reakce se vyskytují například v Krebsově cyklu, při β-oxidaci mastných kyselin či desaturačních reakcích, které mají za cíl syntézu nenasycených MK.
b) Vzájemné přeměny alkoholů – aldehydů / ketonů – karboxylových kyselin
Trojice skupin organických sloučenin alkoholy, karbonylové sloučeniny a karboxylové kyseliny tvoří řadu vzájemně se lišící stupněm oxidace / redukce. Obecné schéma jejich vzájemné přeměny je následující (směrem ke karbonylové sloučenině a karboxylové kyselině probíhá oxidace, směrem opačným redukce):
1. Primární alkohol ↔ aldehyd ↔ karboxylová kyselina
R-CH2-OH ↔ R-CHO ↔ R-COOH
2. Sekundární alkohol ↔ keton
R1-CH(OH)-R2 ↔ R1-CO-R2
3. Terciární alkohol – nelze zoxidovat
Jako příklad oxidace nám může posloužit vznik dihydroxyacetonfosfátu (DHA-P) z glycerol-3-fosfátu (kofaktorem je FAD), přes který vstupuje glycerol dle aktuálních potřeb organismu do glykolýzy či do glukoneogeneze.
3) Esterifikace
Esterifikace je reakce karboxylové kyseliny s alkoholem, při které vzniká ester a voda:
R1-OH + R-COOH → R1–O-(C=O)-R + H2O
Nejvýznamnější karboxylové kyseliny, jejich anionty a acyly shrnují následující tabulky.
1) Nasycené monokarboxylové kyseliny
|
C |
Systematický název |
Triviální název |
Latinský název |
Acyl |
Aniont |
| 1 | metanová | mravenčí | ac. formicum | formyl | formiát |
| 2 | etanová | octová | ac. aceticum | acetyl | acetát |
| 3 | propanová | propionová | ac. propionicum | propionyl | propionát |
| 4 | butanová | máselná | ac. butyricum | butyryl | butyrát |
| 5 | pentanová | valérová | ac. valericum | valeryl | valerát |
| 12 | dodekanová | laurová | ac. lauricum | lauryl | laurát |
| 16 | hexadekanová | palmitová | ac. palmiticum | palmitoyl | palmitát |
| 18 | oktadekanová | stearová | ac. stearicum | stearoyl | stearát |
2) Nasycené dikarboxylové kyseliny
|
C |
Systematický název |
Triviální název |
Latinský název |
Acyl |
Aniont |
| 2 | etandiová | štavelová | ac. oxalicum | oxalyl | oxalát |
| 3 | propandiová | malonová | ac. malonicum | malonyl | malonát |
| 4 | butandiová | jantarová | ac. succinicum | sukcinyl | sukcinát |
| 5 | pentandiová | glutarová | ac. glutaricum | glutaryl | glutarát |
| 6 | hexandiová | adipová | ac. adipicum | adipoyl | adipát |
3) Nenasycené monokarboxylové kyseliny
|
C |
Systematický název |
Triviální název |
Latinský název |
Acyl |
Aniont |
| 18:1 | cis-oktadec-9-enová | olejová | ac. oleicum | oleoyl | oleát |
| 18:2 (ω-6) | cis,cis-oktadeka-9,12-dienová | linolová | ac.linoleicum | linoloyl | linolát |
| 18:3 (ω-3) | cis,cis,cis-oktadeka-9,12,15-trienová | linolenová | ac.linolenicum | linolenoyl | linolenát |
| 20:4 (ω-6) | cis,cis,cis,cis-eikosa-5,8,11,14-tetraenová | arachidonová | ac. arachidonicum | arachidonyl | arachidonát |
4) Nenasycené dikarboxylové kyseliny
|
C |
Systematický název |
Triviální název |
Latinský název |
Acyl |
Aniont |
| 4 | cis-butendiová | maleinová | ac. maleicum | maleinyl | maleinát |
| 4 | trans-butendiová | fumarová | ac. fumaricum | fumaroyl | fumarát |
5) Deriváty karboxylových kyselin
|
C |
Systematický název |
Triviální název |
Latinský název |
Acyl |
Aniont |
| 3 | 2-oxopropanová | pyrohroznová | ac. pyruvicum | pyruvyl | pyruvát |
| 3 | 2-hydroxypropanová | mléčná | ac. lacticum | laktoyl | laktát |
| 4 | 3-oxobutanová | acetooctová | acetoacetyl | acetoacetát | |
| 4 | 3-hydroxybutanová | β-hydroxymáselná | β-hydroxybutyrát | ||
| 4 | 2-hydroxybutandiová | jablečná | ac. malicum | maloyl | malát |
| 4 | 2-oxobutandiová | oxaloctová | oxalacetát | ||
| 5 | 2-oxopentandiová | α-ketoglutarová | α-ketoglutaryl | α-ketoglutarát | |
| 6 | 2-hydroxypropan-1,2,3-trikarboxylová | citrónová | ac. citricum | citrát |
Hydroxykyseliny a ketokyseliny
Vzájemná přeměna hydroxykyselin (které mimo skupinu -COOH obsahují v řetězci i -OH skupinu nahrazující jeden -H) a ketokyselin (nazývaných také oxokyseliny, obsahují v řetězci mimo skupinu -COOH i skupinu =O nahrazující jeden -H) je v metabolických drahách relativně běžná. Příklady oxidací hydroxykyselin na ketokyseliny, či naopak redukcí ketokyselin na hydroxykyseliny zachycují následující schémata.
V metabolismu se vyskytuje i jev keto-enol tautomerie, kde do sebe vzájemně přecházejí dvě formy organických sloučenin: keto- (či také oxo- forma) – obsahující dvojnou vazbou vázaný kyslík jako skupinu =O a enol- forma, kde je dvojná vazba mezi uhlíky a na jeden z nich se pak váže -OH skupina (C=C-OH). Jejich vzájemná přeměna představuje migraci atomu vodíku či protonu, doplněnou prohozením jednoduché vazby a k ní přiléhající vazby dvojné.
Aminokyseliny a oxokyseliny
Aminokyseliny a oxokyseliny představují substituční deriváty karboxylových kyselin. Aminokyseliny obsahují v řetězci kromě -COOH skupiny i skupinu -NH2 , oxokyseliny skupinu =O. Jejich vzájemné přeměny jsou v organismu časté, dochází při nich ke změně -NH2 skupiny na skupinu =O a naopak. Tyto přeměny vykonávají dvě základní reakce:
1) Transaminace
2) Oxidační deaminace
1) Transaminace
Při této reakci je aminokyselina donorem -NH2 skupiny pro oxokyselinu. Z příslušné oxokyseliny vzniká aminokyselina a původní aminokyselina se stává oxokyselinou:
AK1 + OxoK2 ↔ OxoK1 + AK2
2) Oxidační deaminace
Jedná se o reakci vzniku oxokyseliny z aminokyseliny odstraněním -NH2 skupiny, jež se uvolňuje jako amoniak (NH3). Oxidační deaminace patří k významným reakcím, skrze které zahajují aminokyseliny proces svého odbourávání. V lidském těle probíhají zejména v játrech a uvolněný amoniak vstupuje do procesu syntézy močoviny.
Uvedenou reakci katalyzuje glutamátdehydrogenáza.
Dekarboxylace a karboxylace
Během chemické reakce zvané dekarboxylace dochází k odstranění karboxylové skupiny, která se uvolní v podobě molekuly CO2 a je nahrazena protonem. V organismu probíhá jako součást:
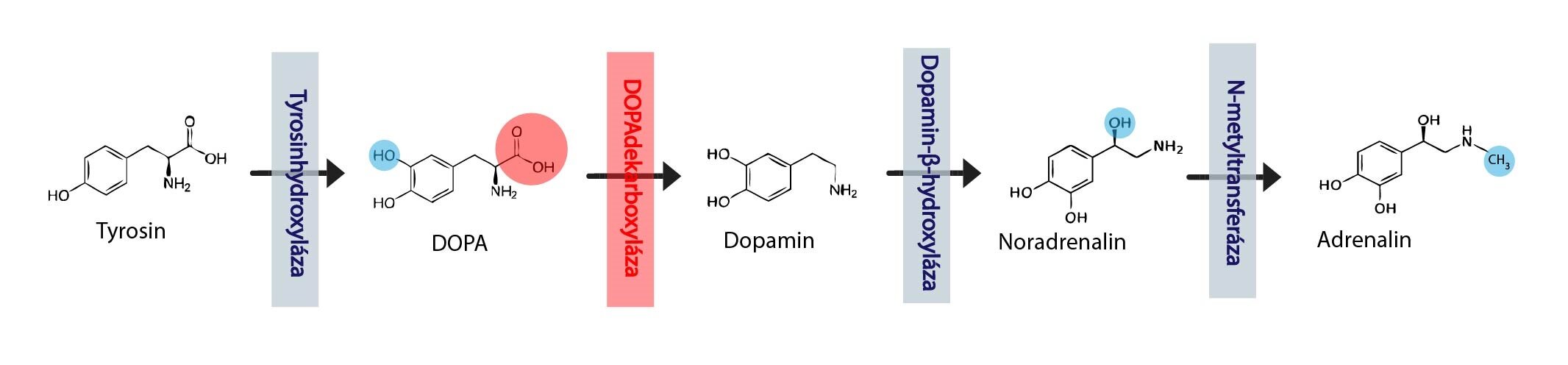
1) Přeměny aminokyselin na biogenní aminy (např. při syntéze mnoha neurotransmiterů)
2) Dehydrogenace 2-ketokyselin – pyruvátdehydrogenázová reakce a dvě reakce Krebsova cyklu
Karboxylace je reakce opačná, dochází při ní k vnesení -COOH skupiny do molekuly. Vyskytuje se například při:
1) Syntéze mastných kyselin
2) Glukoneogenezi
Základy regulace metabolických drah
Regulační reakce konkrétní metabolické dráhy je obvykle lokalizována na jejím začátku – typicky to bývá první irreverzibilní krok. Důvodem je snaha omezit plýtvání zdrojů a zbytečnou produkci meziproduktů, k níž by docházelo, kdyby se dráha zastavila až uprostřed, nikoli na svém začátku.
Regulační enzym bývá přítomný v nízké koncentraci (nižší, než je koncentrace jiných enzymů dráhy), která ho limituje. Obvykle se navíc jedná o allosterický enzym pracující na principu „všechno, nebo nic“. Pro regulaci je totiž výhodné, existuje-li jakýsi koncentrační limit, nad kterým se reakce nastartuje a rychle dosáhne maximální rychlosti, a naopak pod nímž reakce téměř neprobíhá.
V regulaci metabolických drah se (jako i v jiných regulovaných dějích v organismu) uplatňuje princip zpětné vazby (feedback). Při něm dochází ke zpětnému ovlivnění průběhu reakce některým z vytvořených meziproduktů nebo konečným produktem. Rozlišujeme dva druhy zpětné vazby:
1) Negativní zpětná vazba
Odchylka od nastavené hodnoty (set point) vede k sledu reakcí, při nichž se systém vrátí k původní hodnotě. Toto je zdrojem stability systému (který se neustále zpětně vrací k hodnotě set pointu), a negativní zpětná vazba je proto součástí většiny drah.
Jako příklad může sloužit enzym ALA-syntáza I (regulační enzym syntézy hemu lokalizovaný v játrech), který je přes negativní feedback zpětně inhibován produktem celé dráhy – hemem.
2) Pozitivní zpětná vazba
Odchylka od nastavené hodnoty (set point) vede ke sledu reakcí, které ji ještě více prohloubí. Hrozí ovšem riziko vzniku bludného kruhu (circulus vitiosus), při němž každé další zvětšení odchylky její zvětšování ještě urychluje, až nakonec nestabilita systému způsobí jeho kolaps.
Nejtypičtější příklad pozitivní zpětné vazby v organismu najdeme v podobě oxytocinu. Jde o hormon hormon produkovaný v jádrech hypotalamu, který (kromě jiného) vyvolává kontrakce hladké svaloviny dělohy a umožňuje tím průběh porodu. Každá kontrakce prostřednictvím aktivace mechanoreceptorů děložní stěny působí jako stimul pro další sekreci oxytocinu, a jeho efekt tak neustále narůstá až do doby, kdy jsou dítě a následně i placenta porozeny a tlak na děložní stěnu opět klesne.
Regulační krok ovlivňuje:
1) Změna absolutní koncentrace enzymu (množství enzymu)
Ovlivňuje se proces transkripce a translace, a to ve smyslu indukce (aktivace) nebo represe (inhibice) exprese genu kódujícího daný enzym. Příkladem je substrátová indukce, kdy přítomnost substrátu indukuje syntézu enzymu.
2) Modulace aktivity již existujícího enzymu (aktivita enzymu)
a) přítomnost aktivátorů / inhibitorů
b) kovalentní modifikace molekuly enzymu (fosforylace / defosforylace, tvorba aktivních enzymů z proenzymů, …)
_
Autor podkapitoly: Petra Lavríková